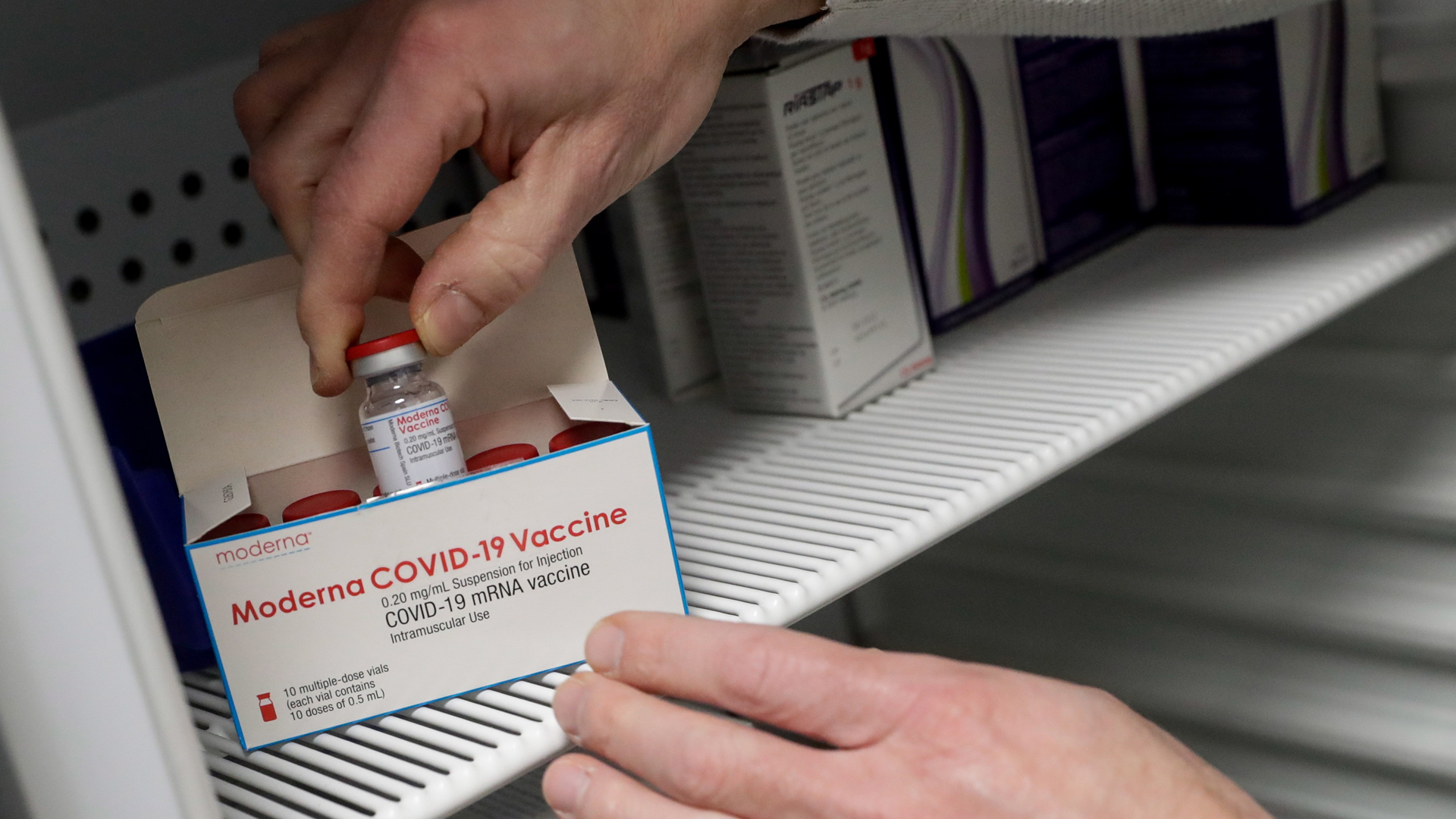
La EMA revisará los datos sobre la vacuna Spikevax de Moderna para determinar si respaldan su seguridad y eficacia en niños de 6 a 11 años
La Agencia Europea de Medicamentos (EMA) comenzó a evaluar la posible extensión de la licencia europea de Moderna a niños de entre 6 y 11 años, una vacuna autorizada en la actualidad solo para mayores de 12 años.
El comité de medicamentos humanos (CHMP) de la EMA revisará los datos sobre la vacuna Spikevax de Moderna para determinar si respaldan su seguridad y eficacia contra COVID-19 en esa franja de edad, lo que incluye los resultados de un estudio clínico en curso.
La agencia espera concluir su evaluación de estos datos en “aproximadamente dos meses” y decidirá si recomendar la extensión del uso de esta vacuna a menores de entre 6 a 11 años, dependiendo de si los datos disponibles son suficientes o se necesitará más información o análisis complementarios.
Cuando termine de evaluar los datos, la EMA comunicará los resultados a la Comisión Europea, que es quien tiene la última palabra sobre la extensión de la licencia.
Moderna recibió su licencia europea para el uso de su vacuna contra COVID-19 en adultos el pasado enero, lo que después se extendió a los adolescentes de más de 12 años en julio.
Las vacuna de ARNm de Pfizer/BioNtech y Moderna son los únicos dos preparados contra COVID-19 que se están utilizando en la actualidad en adolescentes mayores de 12 años en la Unión Europea (UE).
Pfizer, la vacuna más utilizada en la UE desde su aprobación en diciembre del año pasado, también solicitó a la EMA extender su licencia a niños de 5 a 11 años y la agencia espera concluir la evaluación de los datos presentados por la farmacéutica el próximo diciembre, convirtiendo a esta vacuna en la primera en usarse en esa franja de edad en la UE.
Los países europeos están utilizando en sus campañas de vacunación un total de cuatro vacunas contra la covid-19: Pfizer/BioNTech, Moderna, AstraZeneca y Janssen, de la estadounidense Johnson & Johnson.
Más allá de las vacunas, la EMA está centrada ahora en la evaluación de posibles tratamientos para pacientes con COVID-19, entre ellos el antiviral molnupiravir, un fármaco oral prometedor, desarrollado por la farmacéutica estadounidense Merck Sharp & Dohme en colaboración con la biotecnológica Ridgeback Biotherapeutics.
Según sugieren los resultados de los ensayos clínicos, puede reducir la capacidad del SARS-CoV-2 de multiplicarse en el cuerpo, evitando la hospitalización o muerte en adultos contagiados.
De forma paralela a la revisión continua de los datos sobre este fármaco (lo que podrá conducir eventualmente a una licencia europea), la EMA está revisando la información de este antiviral para ayudar a las autoridades nacionales con consejos científicos que les permitan decidir sobre su uso de emergencia antes de su autorización oficial.
Los jefes de las diferentes agencias de medicamentos (HMA) en la UE han acordado con la EMA que hay una “necesidad de orientación adicional” sobre los tratamientos de COVID-19 debido a las crecientes tasas de contagios y decesos por la enfermedad causada por el coronavirus en la UE.
Con información de EFE





