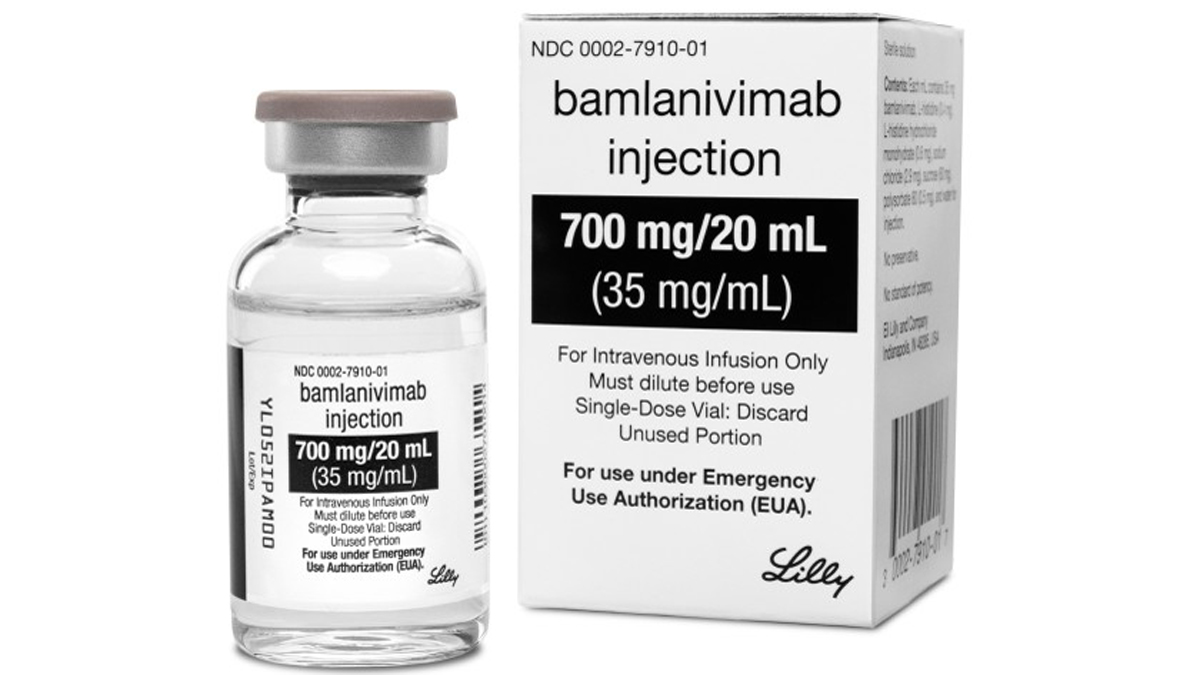
La FDA autorizó de emergencia el uso de Bamlanivimab para tratar el COVID-19. El Gobierno de Estados Unidos destinará 300 mil dosis
La Administración de Drogas y Alimentos de Estados Unidos (FDA) concedió una autorización de uso de emergencia para tratar el COVID-19 con anticuerpos monoclonales.
El tratamiento Bamlanivimab de la compañía Eli Lilly se utilizará en adultos y menores de edad, de al menos 12 años y que pesen al menos 40 kilos, con casos moderados de la enfermedad y alto riesgo de ser hospitalizados.
Aunque se sigue evaluando la seguridad y eficacia de la terapia, en ensayos clínicos demostró reducir las hospitalizaciones por COVID-19.
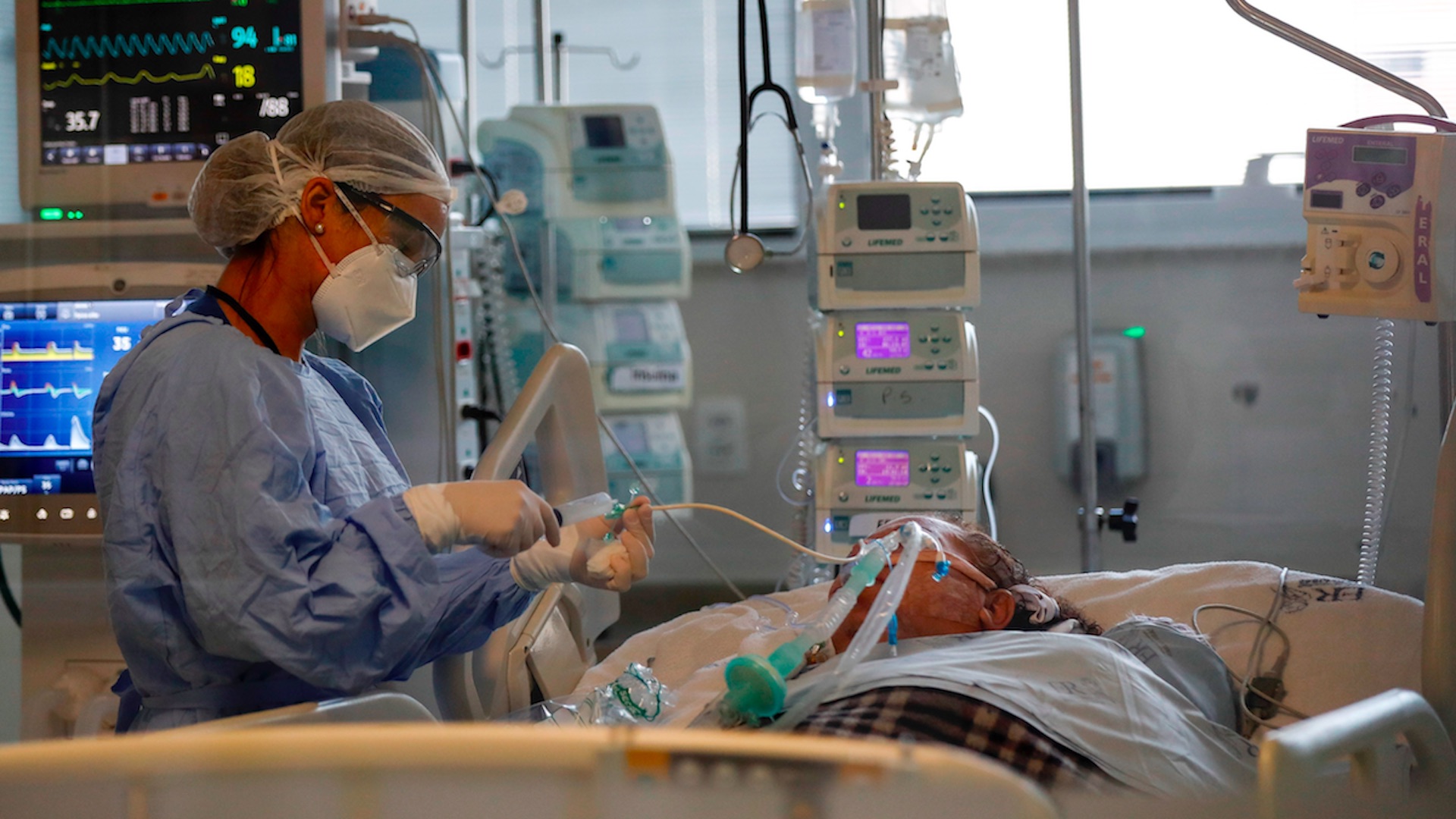
Sin embargo, Bamlanivimab no podrá ser utilizado en pacientes ya hospitalizados o que requieran terapia de oxígeno debido a que puede derivar en complicaciones.
La FDA detalló que los anticuerpos monoclonales son proteínas elaboradas en laboratorio que imitan la capacidad del sistema inmunológico para combatir antígenos dañinos como los virus.
Bamlanivimab es un anticuerpo monoclonal que se dirige específicamente contra la proteína del SARS-CoV-2, diseñado para bloquear la unión del virus y su entrada en las células humanas”, refirió.
Patrizia Cavazzoni, directora interina del Centro de Evaluación e Investigación de Medicamentos de la FDA, señaló que la autorización de emergencia de la nueva terapia servirá a los médicos de primera línea para tratar el coronavirus.
Con base en la revisión de la FDA de la totalidad de la evidencia científica disponible, la agencia determinó que es razonable creer que Bamlanivimab puede ser eficaz en el tratamiento de pacientes no hospitalizados con COVID-19 leve o moderado”, añadió la Administración.
Por su parte, la compañía Eli Lilly dijo que su tratamiento se debe administrar lo más pronto posible después de una prueba COVID-19 positiva y dentro de los 10 días posteriores al inicio de síntomas.
En una primera etapa, el Gobierno de Estados Unidos destinará 300 mil dosis de Bamlanivimab para pacientes de alto riesgo, sin que estos tengan que pagar por el medicamento.
La compañía prevé fabricar hasta un millón de dosis del tratamiento para finales de 2020 y que su uso inicie en el primer trimestre de 2021.
Con información de López-Dóriga Digital