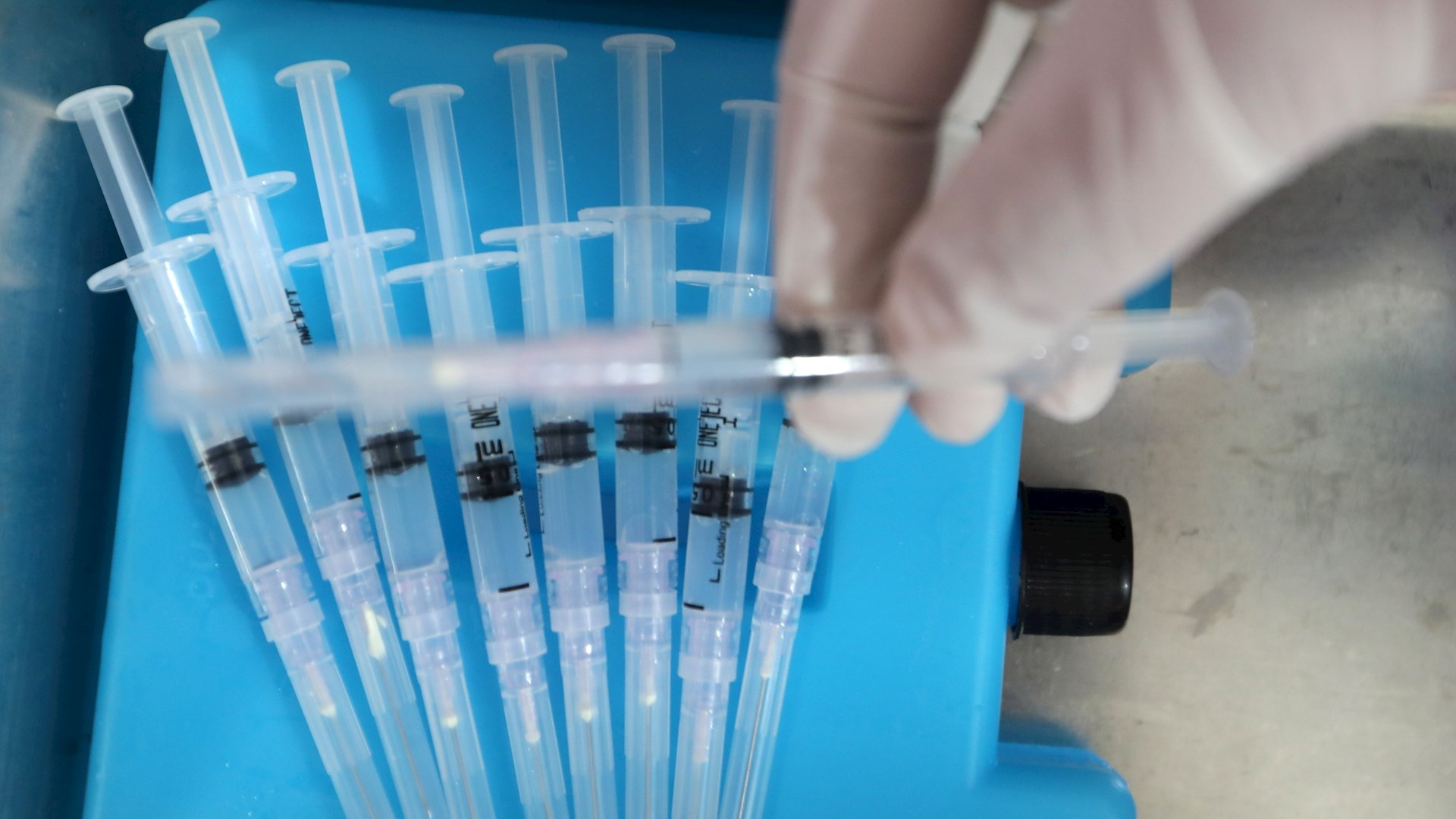
Brasil autorizó el inicio de los ensayos clínicos en fase 1 y 2 de la Butanvac, la primera vacuna contra COVID-19 desarrollada en el país
La Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil autorizó este miércoles el inicio de los ensayos clínicos en fase 1 y 2, con humanos, de la Butanvac, la primera vacuna contra COVID-19 desarrollada en el país y producida por el Instituto Butantan.
El regulador concedió el permiso para que el Instituto Butantan, vinculado a la Gobernación del estado de Sao Paulo y uno de los centros de investigación médica más prestigiosos del país, realice la primera de las tres partes de los test con 400 voluntarios iniciales, de un universo de 6 mil previstos para todo el estudio.
Según señaló Anvisa en una nota oficial, antes de arrancar la vacunación de los voluntarios, el instituto tendrá que presentar algunas “informaciones complementarias” referentes a las pruebas que ha realizado con el antígeno hasta el momento.
Enseguida Butantan podrá iniciar la aplicación experimental de la Butanvac”, agregó.
Se trata de la primera vez que la vacuna, cuyas dos dosis necesarias serán aplicadas con un intervalo de 28 días, será probado en humanos, por lo que el protocolo establece estudios de fase 1 y 2 con un grupo menos numeroso de voluntarios.
El Butantan había solicitado el permiso de Anvisa para iniciar las pruebas el pasado abril, pero la máxima autoridad sanitaria del país pidió informaciones adicionales sobre la fórmula varias veces.
Así, la agencia aseguró este miércoles que, antes de conceder la autorización para el ensayo clínico, fue realizado en los últimos dos meses un “intenso intercambio de informaciones y reuniones” a fin de que “todos los aspectos del estudio estuvieran claros y con garantías de seguridad a los voluntarios”.
A la espera de la anuencia por parte de la agencia reguladora, el Butantan ya había iniciado la producción de la Butanvac y cuenta con unas siete millones de dosis listas, que “serán almacenadas y suministradas a la población después de la autorización definitiva de uso de Anvisa”, según explicó la entidad en su momento.
Por su parte, el gobernador de Sao Paulo, Joao Doria, calificó el aval de Anvisa como una “gran noticia”.
Anvisa acaba de autorizar los test clínicos con la ButanVac, la vacuna del Butantan contra COVID-19, que no depende de insumos de otros países para su producción”, celebró a través de una publicación subida en su cuenta de Twitter.
Además de la Butanvac, el Instituto paulista es el responsable de la producción en Brasil de la Coronavac, la fórmula anticovid desarrollada por el laboratorio chino Sinovac y que es una de las más usadas en el país, uno de los más azotados por el coronavirus en el mundo.
Según los datos más recientes difundidos por el Ministerio de Salud, Brasil, con unos 212 millones de habitantes, ya acumula casi 480 mil muertes y 17.1 millones de infectados.
Con información de EFE





